News Center
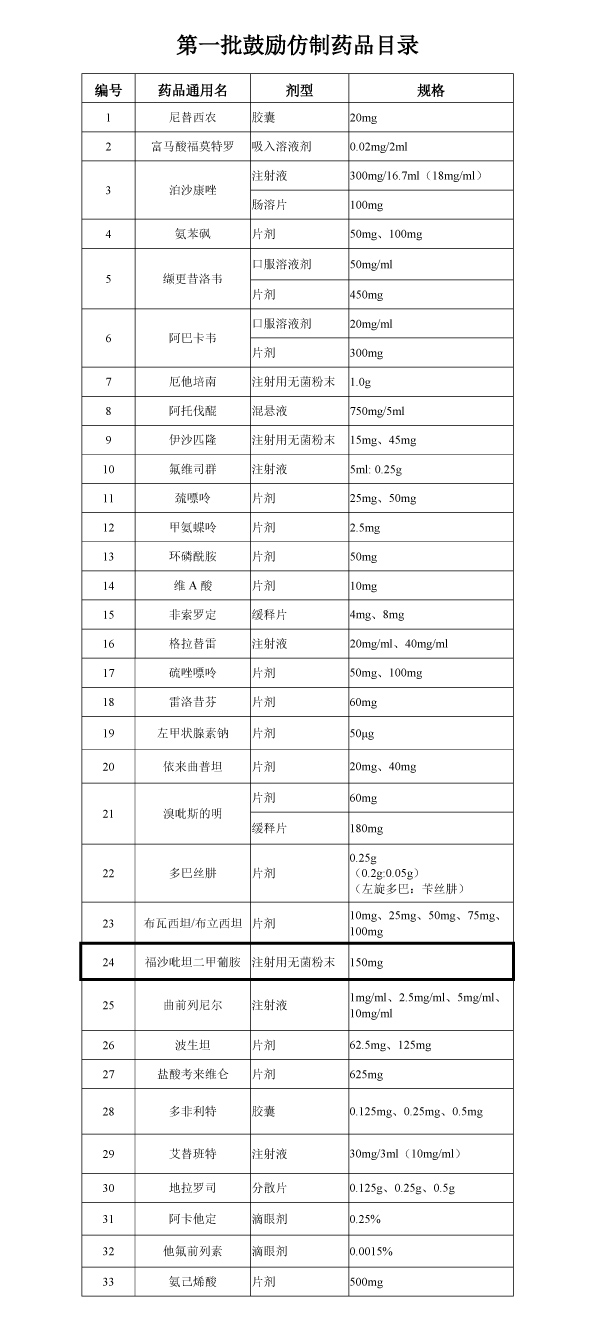
2019年9月17日,國家衛生健康委辦公廳、科技部辦公廳、工業和信息化部辦公廳、國家藥監局綜合司、國家知識產權局辦公室等部委聯合發文,公布《第一批鼓勵仿制藥品目錄》,要求各相關部門按照有關規定,在臨床試驗、關鍵共性技術研究、優先審評審批等方面予以支持。“福沙吡坦二甲葡胺”名列其中(福沙吡坦,又名福沙匹坦,英文名Fosaprepitant,FDA上市的是Fosaprepitant dimeglumine,中文名為福沙匹坦二甲葡胺)。
景峰醫藥副總裁兼董事會秘書畢元女士表示,福沙匹坦是一種腫瘤輔助用藥,主要用于腫瘤治療過程中化療的輔助用藥,防止化療引起的惡心、嘔吐等。數據顯示,福沙匹坦為美國市場上的次級重磅產品,其市場規模在2018年超過了3.5億美元。
默沙東原研藥Emend的橙皮書專利于2019年9月4日到期,景峰醫藥控股子公司Sungen Pharma(尚進)于2019年9月5日獲得其仿制藥ANDA批準,為該市場中首批獲批企業。(詳見公司公告【2019—067】)目前,公司正積極準備相關產品的中美雙申報工作,力爭早日實現國內國際兩個市場齊頭并進。
此次《第一批鼓勵仿制藥品目錄》的公布,將有效提升景峰醫藥相關產品的研發、生產進程,對于公司拓展市場、提升業績、加速國際化布局帶來積極影響。
——董秘處 俞志豪